- 首页
- 我们的服务
-
项目简介
医疗器械检测是确保产品安全、有效与合规的关键环节,涵盖性能验证、材料安全及生物相容性测试,旨在预防潜在风险,保护患者健康,推动行业持续发展。
服务项目
医用敷料类、医用输注器具及医用导管类、药械组合医疗器械、医美产品
服务优势
资质完备:已获得国家CMA、省级CMA及CNAS资质,检测结果权威可靠。
项目全面:提供理化/微生物检测、生物相容性研究(依据GB/T 16886/ISO 10993)及临床前功能性评价的一站式服务。
专业团队:拥有经验丰富的检测队伍,精通各类医疗器械标准与流程,确保高效精准服务。
风险控制:通过体外/体内实验综合评价产品安全性,助力产品合规上市,提升市场竞争力。
-
服务简介
华微检测是由广州高新区投资集团直属单位联合华南新药创制中心及海归技术团队共同建设的第三方检测机构,专注生物安全、生物医药与动物实验等领域。我们搭建生物制品分析检测综合平台,严格遵循ISO/IEC17025体系,已获国家CMA和CNAS认证,提供符合《中国药典》要求的细胞系/株全面检定服务,适用于抗体、重组蛋白、疫苗、细胞基因治疗产品等生物制品的合规报批。
服务项目
细胞库检测、生物制品批放行检查/型式检查、细胞内外源病毒因子检查、原辅料/培养基/耗材检查、工艺杂质残留研究、微生态制剂(活菌制剂)检查
服务优势
权威资质:通过CMA、CNAS认证,实验室符合GMP体系,检测结果具法律效力和国际公信力。
高标准实验室:配备多间加强型P2实验室(广州市备案),B+A环境,满足无菌及病毒检测要求。
法规符合性强:严格遵循FDA、CHP、EP、ICH等国际国内法规,建立全面细胞库检定流程。
专业团队与技术:依托高水平技术团队和完备操作规程,为客户提供精准、高效的生物制品检测服务。
-
服务简介
我司提供全面的药代药效学研究评价服务。我们严格遵循NMPA、FDA和ICH相关技术指导原则,为客户提供符合申报要求的全套体内外评价模型与试验数据支持。
服务项目
药代动力学研究、 药效学研究、皮肤外用试剂透皮吸收研究
服务优势
综合平台:整合药代、药效及透皮研究能力,提供从体外到体内的一体化评价方案。
专业团队:拥有经验丰富的研究人员,精通各类药物剂型与模型的评价标准与法规要求。
先进设备:配备LC-MS/MS、高效渗透系统等先进仪器,保证数据精准、可靠。
合规高效:实验过程严格遵循GLP规范,支持国内外注册申报,加速产品研发与上市进程。
-
服务简介
华微检测提供专业的药品及原辅料质量研究与检测分析服务,配备精密仪器实验室、核磁共振实验室及多类先进分析设备,涵盖理化性质分析、杂质研究、含量测定及方法开发与验证等项目,全面支持药品研发、生产及注册申报的质量控制需求。
服务项目
药品/原辅料理化检查、药品微生物检查、效价与生物学活性、生物安全性检测(生物制品)、抗菌/抗病毒药物筛选
服务优势
设备先进齐全:配置HPLC、LC-MS、GC-MS、ICP-MS、AAS、酶标仪等多类型高端仪器,保证检测数据精准可靠。
技术能力深厚:具备药品及原辅料方法开发与验证经验,可提供从常规检测到复杂研究的全流程解决方案。
定制化服务:依据企业实际需求,提供灵活、高效的定制化开发与检测服务,助力企业加速研发进程。
平台资源丰富:依托完备的实验室平台和专业团队,能够同时应对多品类、多标准的药品质量评价任务
-
服务简介
新型冠状病毒疫情严重危害人类健康,已成为全球关注的公共卫生问题。抗病毒材料作为一种重要的防护手段,可有效抑制和杀灭病毒,但其实际效果需通过专业检测验证。 随着疫情防控常态化,市场对消毒及健康防护产品的需求持续增长,相关企业对于产品检测的需求也日益迫切。 华微检测为企业提供抗病毒材料及病毒消杀产品的专业检测服务,助力产品有效性验证,为公共健康保驾护航。
服务项目
净化产品病毒去除性能测试、消毒产品病毒灭活效果测试、日化轻工材料抗病毒效果测试、精品定制化服务
服务优势
精英团队,背景多元:技术团队由广微所、华南新药创制中心、高校重点实验室人员及病毒学领域海归博士专家组成,结构合理、实战经验丰富。
顶尖设备,科研级服务:依托先进硬件设施与高层次科研队伍,在常规检测中提供深度、沉浸式的科研体验。
灵活定制,一站式支持:除标准化测试外,支持各类客供实验方案,为产品开发与课题研究提供精品化、全方位技术服务。
-
服务简介
食品保健品检测是通过理化、微生物与毒理学等方法,对食品及保健品的成分、安全性、功效及标签合规性进行全面分析的科学过程。 我们致力于通过检测重金属、农残、微生物等风险物质,保证产品安全;验证有效成分与宣称功能,确保功效可信
服务项目
食品保健品毒理学检测、食品保健品功效评价研究、其它定制化服务
服务优势
符合国家标准与国际法规,助力市场准入; 具第三方检测报告,增强消费者信任,提升产品竞争力。
-
华微检测除核心检测服务外,还可提供以下延伸技术支持:专业实验空间租赁、定制化实验方案设计、规范化的实验动物代养 实验方案设计是决定科研成败与数据可靠性的关键环节。我们凭借专业团队和丰富经验,协助客户根据研究目标与条件,设计科学、严谨、可操作的实验方案,为项目顺利开展提供坚实基础。
- 新闻资讯
- 检测流程
- 下载中心
- 关于我们
- 联系我们
 新闻资讯INFORMATION CENTER今日知多D之保健食品备案篇
新闻资讯INFORMATION CENTER今日知多D之保健食品备案篇 3238次
3238次 2025-04-16
2025-04-16
2015年修订的《食品安全法》实施,保健食品行业迎来新变革,正式开启注册与备案分类管理新模式,此后,随着《保健食品注册与备案管理办法》、《保健食品备案工作指南》、《保健食品原料目录与保健功能目录管理办法》等配套文件的出台实施,“双轨制”下保健食品注册与备案工作正式拉开帷幕。
而今年3月1日,辅酶Q10等五种保健食品原料目录的正式实施,标志着功能类保健食品原料产品备案工作正式启动,保健食品备案产品不再局限是维生素和矿物质类原料。
保健食品实施备案管理后大大缩短了之前的注册时间,降低了企业成本,更利于企业经营和产品创新。而未来,随着保健食品原辅料目录的不断扩充,更多天然植物提取物的原料将加入备案目录,保健食品备案类产品将越来越多。
哪些保健食品可以实行备案制?保健食品备案流程如何?申报要点、提交材料有哪些等等?下面我们来逐一介绍。
一、哪些保健食品可以备案
依照《保健食品注册与备案管理办法》,生产和进口下列保健食品应当依法备案:
1. 使用的原料已经列入保健食品原料目录的保健食品;
2. 首次进口的属于补充维生素、矿物质等营养物质的保健食品。首次进口的属于补充维生素、矿物质等营养物质的保健食品,其营养物质应当是列入保健食品原料目录的物质。
划重点:以辅酶Q10等五种原料为原料的备案仅针对国产保健食品,不包括首次进口的保健食品。
以辅酶Q10等五种原料为原料的进口保健食品目前监管如下方式进行:
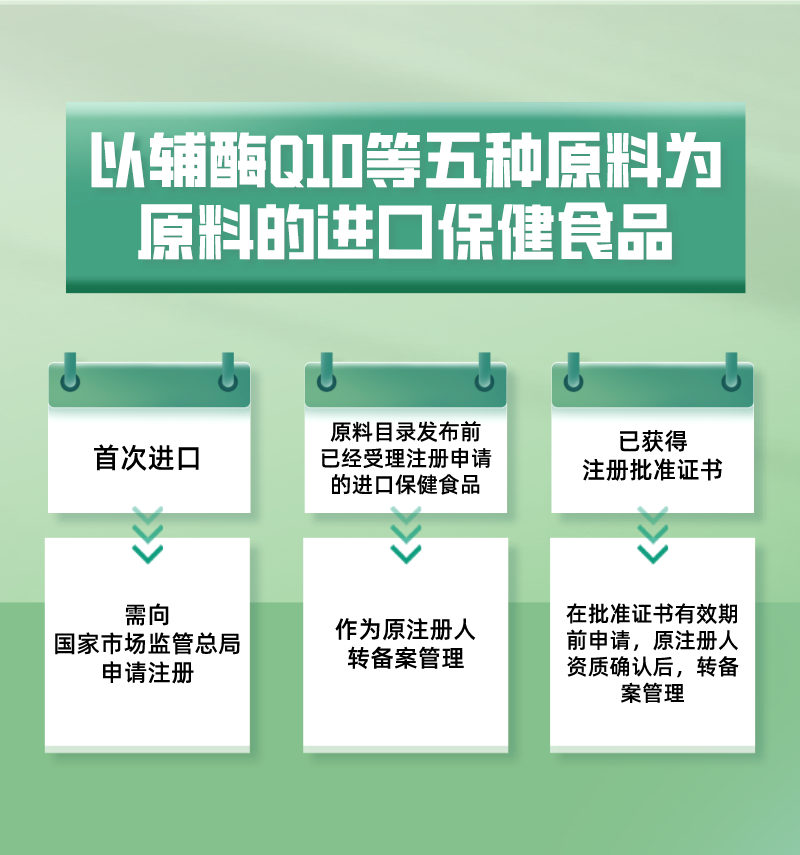
二、保健食品备案主体
1. 国产保健食品
国产保健食品备案人应当是保健食品生产企业,保健食品原注册人可以作为备案人。
原注册人包括:
(1)《保健食品原料目录》发布前受理的保健食品注册申请,其原料已列入原料目录,且符合备案相关技术要求的,申请该产品备案的原注册申请人;
(2)获得注册的保健食品,其原料已列入《保健食品原料目录》,且符合备案相关技术要求的,申请该产品备案的原注册人;
(3)《保健食品原料目录》发布前受理的保健食品注册申请,以及获得注册的保健食品,其原料或用量不完全符合《保健食品原料目录》以及备案技术要求的,注册申请人或证书持有人同意按照《保健食品原料目录》调整产品原料和产品技术要求的,也可以作为原注册人。
但是,《保健食品原料目录》发布后受理的注册申请保健食品,其原料已列入《保健食品原料目录》,且产品符合相关技术要求,原注册申请人不可以作为原注册人申请该产品备案。
2. 进口保健食品
进口保健食品的备案人,应当是上市保健食品境外生产厂商。
三、保健食品备案相关法律法规
名称
发布日期
施行日期
1
*人民共和国食品安全法(2018年修订版)
2018.12.29
2018.12.29
2
保健食品注册与备案管理办法(2020年修订版)
2020.11.03
2020.11.03
3
保健食品备案工作指南(试行)
2017.05.02
2017.05.02
4
保健食品标注警示用语指南
2019.06.10
2019.08.20
5
保健食品命名指南(2019年版)
2019.11.10
2019.11.12
6
保健食品原料目录-营养素补充剂(2020年版)
2020.12.01
2021.03.01
7
辅酶Q10等五种保健食品原料目录
2020.12.01
2021.03.01
8
辅酶Q10等五种保健食品原料备案产品剂型及技术要求
2021.01.29
2021.06.01
9
保健食品备案产品可用辅料及其使用规定(2021年版)
2021.02.20
2021.06.01
10
保健食品备案产品剂型及技术要求(2021年版)
2021.02.20
2021.06.01
四、保健食品备案流程及所需材料
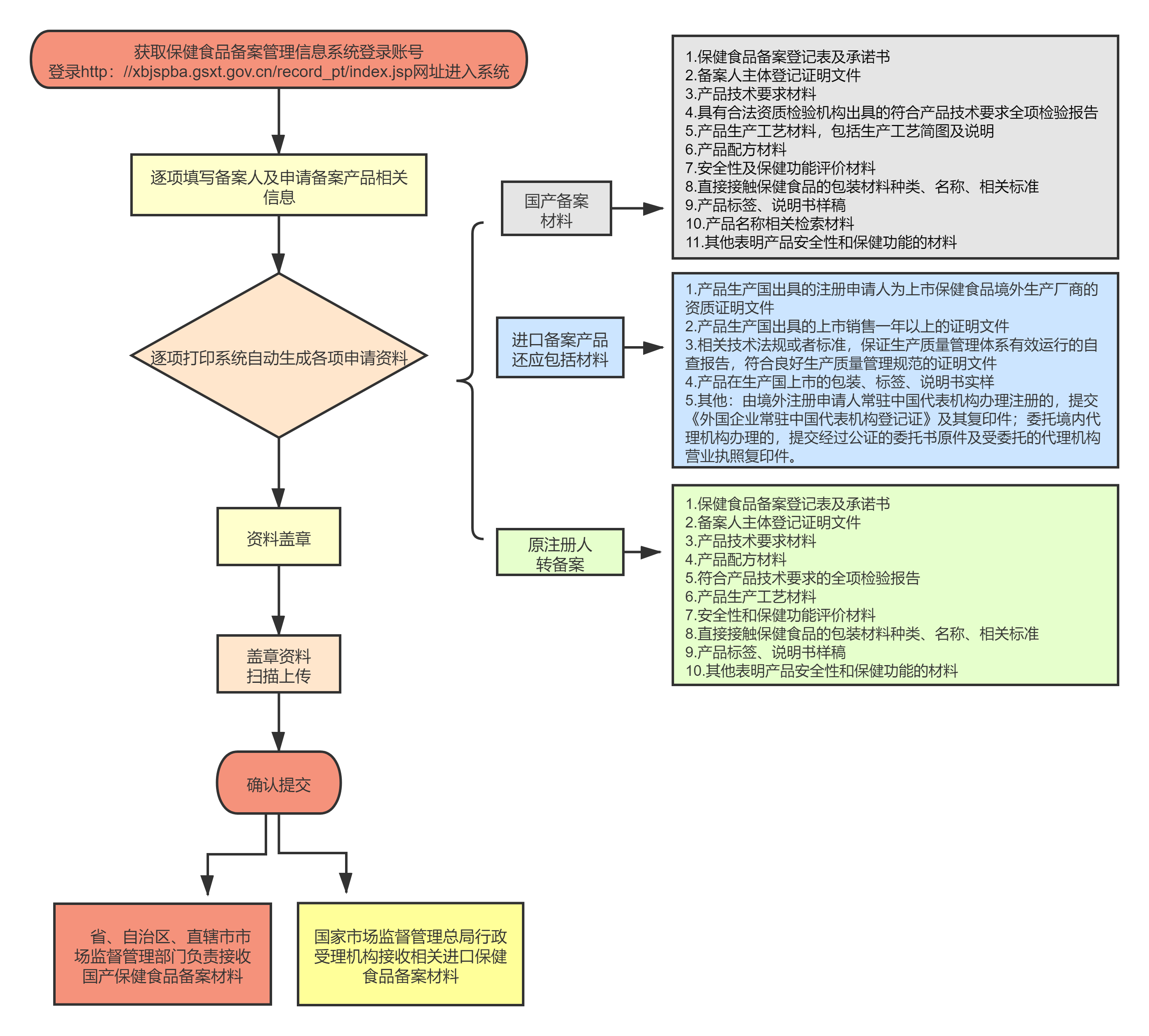
广东省华微检测股份有限公司(华微检测)为广州市微生物研究所、广东华南新药创制中心及高水平技术团队共建的专门从事生物安全、生物医药及保健品等领域的第三方检测机构。华微检测实验室严格遵照ISO/IEC17025、RB/T214等标准、规范要求运行,并已取得第三方检测机构相关认证证书,在保健食品领域,可为客户提供从原料到产品、从注册备案咨询到代理申报、从动物毒理检测到功效评价等“一站式”、“全流程”的检测、咨询及申报服务。

- 服务范围
特色检测服务 +
微生物制剂评价
抗菌抗病毒药物筛选
抗生素效价检测
医疗器械检测 +
医用敷料检测
医用输注器具及医用导管检测
药械组合医疗器械检测
医美产品检测
生物制品检测 +
细胞库检测
生物制品批放行检查/型式检查
细胞内外源病毒因子检查
原辅料、培养基、耗材检查
工艺杂质残留研究
微生态制剂(活菌制剂)检查
非临床研究与生物样本检测 +
药代动力学研究
药效学研究
皮肤外用制剂透皮吸收研究
样本分析检测
病毒中和抗体检测
药品检测 +
药品、原辅料理化检查
药品微生物检查
效价与生物学活性
抗菌/抗病毒药物筛选
药包材检测
病毒杀灭检测 +
净化产品病毒去除性能测试
消毒产品病毒灭活效果测试
日化轻工材料抗病毒效果测试
精品定制化测试
食品/保健食品检测 +
食品保健品毒理学检测
食品保健品功效评价研究
其它定制化服务
其他检测服务 +
化妆品原料毒理检测
化妆品体外功效评价
化妆品/美容仪体内外透皮吸收评价
实验动物饲/寄养服务
动物诱发性造模
仪器设备共享服务
分子生物学实验技术服务平台
ELISA实验技术服务
荧光定量PCR实验技术服务
Western Blotting实验技术服务
外源性生物残留检测服务平台
病毒核酸参考品服务
- 联系我们
- 联系人:史工18928790749、严工
- 手机:19924323595、020-82118202、020-31608627【微信同号】
- 微信号:
扫码添加史工 扫码添加严工
- 邮箱:yanyongxian@gdhvt.com
- 地址:广州市黄埔区揽月路3号F栋316(总部)广州市黄埔区科学城尖塔山路1号(动物中心)

 为您推荐更多
为您推荐更多

扫码添加史工 扫码添加严工
联系人:史工18928790749、严工
联系电话:19924323595、020-82118202、020-31608627
地址:广州市黄埔区揽月路3号F栋316(总部)广州市黄埔区科学城尖塔山路1号(动物中心)
版权所有 © 广东省华微检测股份有限公司- 特色检测服务
- 医疗器械检测
- 生物制品检测
- 非临床研究与生物样本检测
- 药品检测
- 病毒杀灭检测
- 食品/保健食品检测
- 其他检测服务
-




 立即咨询
立即咨询 留言咨询
留言咨询









